Anti-Hbc: Kháng Thể Kháng Kháng Nguyên Lõi Virus...
Liên hệ
Hà Nội
Antibodies to hepatitis B core antigen (anti-HBc) Catalog Number: 04927826160
Hóa chất có thể được sử dụng trên máy: Elecsys 2010, Modular analytics E170, cobas e 411 cobas e 601
Mục đích sử dụng
Xét nghiệm miễn dịch in vitro dùng để định tính kháng thể IgG và IgM kháng kháng nguyên lõi của vi rút viêm gan B trong huyết thanh và huyết tương người.
Xét nghiệm miễn dịch điện hóa phát quang “ECLIA” được dùng cho các máy xét nghiệm miễn dịch Elecsys và cobas e.
Chứng nhận pháp quy
Xét nghiệm Elecsys Anti-HBc đã được cấp Chứng nhận CE theo Chỉ thị 98/79/EC. Hiệu năng của xét nghiệm đã được thiết lập và chứng nhận bởi cơ quan chức năng đáp ứng Tiêu chuẩn kỹ thuật chung (CTS) cho sản phẩm dùng trong chẩn đoán và sàng lọc máu.
Tóm tắt
Vi rút viêm gan B gồm một vỏ ngoài (HBsAg) và một lõi bên trong (HBcAg).
Kháng nguyên lõi của vi rút viêm gan bao gồm 183-185 acid amin.
Trong thời gian nhiễm vi rút viêm gan B, kháng thể kháng HBcAg được hình thành và thường tồn tại suốt đời. Kháng thể kháng HBc xuất hiện ngay sau khi nhiễm vi rút viêm gan B và thường có thể phát hiện sớm trong huyết thanh ngay sau khi xuất hiện HBsAg. Kháng thể kháng HBc hiện diện cả trong những người đã hồi phục sau nhiễm vi rút viêm gan B và những người đang mang HBsAg trong cơ thể. Vì thế, kháng thể này là chỉ thị cho tình trạng đang hoặc đã từng nhiễm viêm gan B.
Trong một số hiếm trường hợp, nhiễm HBV cũng có thể xảy ra mà không thể phát hiện kháng thể kháng HBc về phương diện miễn dịch (thường thấy ở những bệnh nhân bị ức chế miễn dịch).
Do kháng thể kháng HBc tồn tại lâu dài sau khi nhiễm vi rút viêm gan B, nên sàng lọc kháng thể kháng HBc là nguồn cung cấp thông tin tốt nhất về tần suất viêm gan B trong một nhóm người cụ thể.
Định lượng kháng thể kháng HBc kết hợp với các xét nghiệm viêm gan B khác cho phép chẩn đoán và theo dõi nhiễm HBV. Trong trường hợp không có các dấu ấn viêm gan B nào khác (những người có HBsAg âm tính), kháng thể kháng HBc có thể là dấu ấn duy nhất về việc đang nhiễm vi rút viêm gan B
Nguyên lý xét nghiệm
Nguyên lý cạnh tranh. Tổng thời gian xét nghiệm: 27 phút.
• Thời kỳ ủ đầu tiên: Tiền xử lý 40 µL mẫu với chất khử (Bản quyền số US 6150113 tại Mỹ hoặc EP 0 341 439 B1 tại Châu Âu).
• Thời kỳ ủ thứ hai: Sau khi thêm HBcAg, một phức hợp tạo thành với kháng thể kháng HBc có trong mẫu.
• Thời kỳ ủ thứ ba: Sau khi thêm kháng thể đánh dấu biotin và kháng thể đánh dấu phức hợp rutheniuma đặc hiệu với HBcAg, cùng với vi hạt phủ streptavidin, các vị trí chưa gắn kết trên kháng nguyên HBc bị chiếm giữ. Toàn bộ phức hợp trở nên gắn kết với pha rắn thông qua sự tương tác giữa biotin và streptavidin.
• Hỗn hợp phản ứng được chuyển tới buồng đo, ở đó các vi hạt đối từ được bắt giữ trên bề mặt của điện cực. Những thành phần không gắn kết sẽ bị thải ra ngoài buồng đo bởi dung dịch ProCell. Cho điện áp vào điện cực sẽ tạo nên sự phát quang hóa học được đo bằng bộ khuếch đại quang tử.
• Các kết quả được xác định tự động nhờ phần mềm Elecsys và cobas e bằng cách so sánh tín hiệu điện hóa phát quang thu được từ sản phẩm phản ứng của mẫu với tín hiệu giá trị ngưỡng phản ứng thu được trước đó qua việc chuẩn xét nghiệm anti-HBc.
Thuốc thử - dung dịch tham gia xét nghiệm
M Vi hạt phủ Streptavidin (nắp trong), 1 chai, 6.5 mL: Vi hạt phủ Streptavidin 0.72 mg/mL; chất bảo quản.
R0 DTT (nắp trắng), 1 chai, 5 mL: 1,4-dithiothreitol 110 mmol/L; đệm citrate 50 mmol/L.
R1 HBcAg (nắp xám), 1 chai, 8 mL: HBcAg (E. coli, rDNA), > 25 ng/mL; đệm phosphate 100 mmol/L, pH 7.4; chất bảo quản.
R2 Anti-HBcAg-Ab~biotin; anti-HBcAg-Ab~Ru(bpy)2+3 (nắp đen), 1 chai, 8 mL: Kháng thể đơn dòng kháng HBc đánh dấu biotin (chuột) > 800 ng/mL; kháng thể đơn dòng kháng HBc (chuột) đánh dấu phức hợp ruthenium > 130 ng/mL; đệm phosphate 100 mmol/L, pH 7.4; chất bảo quản.
Cal1 Mẫu chuẩn âm tính 1 (nắp trắng), 2 chai, mỗi chai 1.0 mL: Huyết thanh người, chất bảo quản.
Cal2 Mẫu chuẩn dương tính 2 (nắp đen), 2 chai, mỗi chai 1.0 mL: Kháng thể kháng HBc (người) > 8 PEI U/mLb trong huyết thanh người; chất bảo quản.
b) đơn vị Viện Paul-Ehrlich
Thận trọng và cảnh báo
Dùng trong chẩn đoán in vitro.
Áp dụng các cảnh báo thông thường cần thiết cho việc xử lý các loại thuốc thử phòng thí nghiệm.
Loại bỏ các chất thải tuân theo hướng dẫn của địa phương.
Bảng dữ liệu an toàn hóa chất có sẵn để cung cấp cho chuyên viên sử dụng khi có yêu cầu.
Tất cả các sản phẩm từ người đều có khả năng lây nhiễm.
Tất cả sản phẩm từ máu người đều đã chuẩn bị kỹ từ máu của những người hiến máu đã được xét nghiệm riêng lẻ và cho kết quả âm tính với HBsAg (chỉ Cal1) và kháng thể kháng HCV và HIV.
Các phương pháp xét nghiệm được sử dụng đều đã được FDA chấp thuận hay đã đáp ứng Chỉ thị Châu Âu 98/79/EC, Phụ lục II, Danh mục A.
Huyết thanh chứa kháng thể kháng HBc (Cal2) bị bất hoạt bằng β-propiolactone và tia cực tím.
Tuy nhiên, không có phương pháp bất hoạt hay xét nghiệm nào có thể loại bỏ hoàn toàn nguy cơ lây nhiễm một cách chắc chắn tuyệt đối, nên xử lý cẩn thận như mẫu bệnh phẩm. Trong trường hợp có phơi nhiễm, nên tuân theo hướng dẫn của cơ quan y tế địa phương.
Không nên sử dụng thuốc thử đã hết hạn sử dụng.
Tránh để các dung dịch thuốc thử và các mẫu (mẫu xét nghiệm, mẫu chuẩn và mẫu chứng) bị tạo bọt.
Sử dụng thuốc thử
Thuốc thử trong hộp thuốc thử sẵn sàng để sử dụng và được cung cấp trong các chai tương thích với hệ thống.
Máy phân tích Elecsys 2010 và cobas e 411: Các mẫu chuẩn Cal1 và Cal2 phải đưa về nhiệt độ 20-25 °C trước khi đặt trên thiết bị phân tích để chuẩn. Sau khi sử dụng, đóng ngay nắp chai lại và bảo quản ở 2-8 °C. Đảm bảo không có dung dịch chuẩn nào còn sót lại trên nắp bật đã mở. Do có khả năng xảy ra các hiệu ứng bay hơi, không được thực hiện quá 5 lần quy trình chuẩn trên mỗi bộ chai mẫu chuẩn.
Máy phân tích MODULAR ANALYTICS E170, cobas e 601 và cobas e 602: Ngoại trừ trường hợp cần sử dụng toàn bộ thể tích để chuẩn trên thiết bị phân tích, thông thường nên chuyển phần mẫu chuẩn phụ sẵn sàng để sử dụng vào những chai trống có nắp bật (CalSet Vials). Dán nhãn cho các chai phụ. Bảo quản chai phụ ở 2-8 °C để sử dụng sau này.
Chỉ thực hiện một quy trình chuẩn đối với mỗi chai chuẩn phụ.
Máy phân tích tự động đọc mã vạch trên nhãn thuốc thử và ghi nhận tất cả thông tin cần thiết cho việc chạy thuốc thử.
Bảo quản và độ ổn định
Bảo quản ở 2-8 °C.
Đặt hộp thuốc thửElecsys Anti-HBc (M, R0, R1, R2) theo hướng thẳng đứng nhằm đảm bảo tính hữu dụng của toàn bộ các vi hạt trong khi trộn tự động trước khi sử dụng.
Bảo quản mẫu chuẩn theo hướng thẳng đứng! Đảm bảo không có dung dịch chuẩn nào còn sót lại trên nắp bật đã mở.
Lấy và chuẩn bị mẫu
Chỉ những mẫu được liệt kê dưới đây đã được thử nghiệm với số lượng đầy đủ và được chấp nhận.
Huyết thanh được lấy bằng cách sử dụng các ống chuẩn lấy mẫu hoặc các ống chứa gel tách.
Huyết tương chống đông bằng Na-heparin, K3-EDTA, và natri citrate.
Tiêu chuẩn: Chỉ định đúng mẫu âm tính và dương tính.
Mẫu ổn định trong 5 ngày ở 2-8 °C, 3 tháng ở -20 °C. Mẫu có thể được giải đông 5 lần.
Các loại mẫu phẩm được liệt kê đã được thử nghiệm cùng với bộ các ống nghiệm lấy mẫu chọn lọc, có bán trên thị trường vào thời điểm xét nghiệm, ngh˜ia là không phải tất cả các ống lấy mẫu của các nhà sản xuất đều được thử nghiệm. Các bộ ống chứa mẫu của các nhà sản xuất khác nhau có thể làm từ những vật liệu khác nhau có khả năng ảnh hưởng đến kết quả xét nghiệm trong một số trường hợp. Khi xử lý mẫu trong các ống chính (ống chứa mẫu), phải tuân theo hướng dẫn của nhà sản xuất ống.
Lưu ý! Đặc biệt quan trọng với xét nghiệm Elecsys Anti-HBc: Ly tâm cẩn thận các mẫu đông lạnh, mẫu có chứa kết tủa, và các mẫu được đo lặp lại trước khi thực hiện xét nghiệm.
Có thể sử dụng mẫu bị bất hoạt bởi nhiệt. Không sử dụng mẫu thử và mẫu chứng được ổn định bằng azide.
Đảm bảo nhiệt độ của các mẫu bệnh phẩm, mẫu chuẩn và mẫu chứng ở nhiệt độ phòng (20-25 °C) trước khi tiến hành đo.
Do có khả năng xảy ra các hiệu ứng bay hơi, các mẫu bệnh phẩm và mẫu chuẩn trên các thiết bị phân tích phải được đo trong vòng 2 giờ.
Xét nghiệm
Để tối ưu hiệu năng xét nghiệm, nên tuân theo hướng dẫn trong tài liệu này cho các máy tương ứng. Tham khảo hướng dẫn vận hành cho từng xét nghiệm đặc hiệu tương ứng.
Thiết bị tự động trộn các vi hạt trước khi sử dụng. Máy đọc thông số đặc hiệu của xét nghiệm trên mã vạch của thuốc thử. Trong trường hợp ngoại lệ nếu máy không đọc được mã vạch, hãy nhập chuỗi 15 con số vào.
Máy phân tích MODULAR ANALYTICS E170, cobas e 601 và cobas e 602: Cần có dung dịch PreClean M.
Máy phân tích MODULAR ANALYTICS E170, Elecsys 2010 và cobas e: Đưa thuốc thử đang lạnh về khoảng 20 °C và đặt vào khay chứa thuốc thử (20 °C) trên máy phân tích. Tránh tạo bọt. Hệ thống sẽ tự động điều hòa nhiệt độ của thuốc thử và đóng/mở nắp chai.
Đặt các mẫu chuẩn Cal1 và Cal2 vào vùng đặt mẫu của máy. Chỉ mở nắp trong lúc chuẩn. Tất cả những thông tin cần thiết để thực hiện chuẩn đều được mã hóa trên mã vạch và được đọc tự động. Sau khi hoàn thành chuẩn, lưu trữ Cal1 và Cal2 ở 2-8 °C hoặc loại bỏ chúng (máy phân tích MODULAR ANALYTICS E170, cobas e 601 và cobas e 602).
Chuẩn
Thông tin ghi nhận dữ liệu: Phương pháp này đã được chuẩn hóa theo “HBc-Reference Material 82 (anti-HBc IgG)” của Viện Paul-Ehrlich, Langen (Đức).
Tần suất chuẩn định: Cần thực hiện chuẩn mỗi lô thuốc thử sử dụng Elecsys Anti-HBc Cal1 và Cal2, và hộp thuốc thử mới (nghĩa là không quá 24 giờ từ khi hộp thuốc thử được đăng ký trên máy phân tích).
Thực hiện chuẩn lại khi:
• sau 1 tháng (28 ngày) nếu sử dụng các hộp thuốc thử cùng lô
• sau 7 ngày (nếu sử dụng cùng hộp thuốc thử đó)
• khi cần thiết: ví dụ: khi kết quả mẫu chứng Elecsys
PreciControl Anti-HBc nằm ngoài thang
• thường xuyên hơn khi có các quy định liên quan
Khoảng tín hiệu điện hóa phát quang (chỉ số đo được) cho các mẫu chuẩn:
Mẫu chuẩn âm tính (Cal1):
42000-250000 (máy phân tích Elecsys 2010 và cobas e 411) hoặc 100000-650000 (máy phân tích MODULAR ANALYTICS E170, cobas e 601 và cobas e 602).
Mẫu chuẩn dương tính (Cal2): 100-3000 (máy phân tích Elecsys 2010, MODULAR ANALYTICS E170 và cobas e ).
Kiểm tra chất lượng
Để kiểm tra chất lượng, sử dụng Elecsys PreciControl Anti-HBc.
Chạy các mẫu chứng 1 và 2 tối thiểu là một lần cho mỗi 24 giờ khi xét nghiệm vẫn đang sử dụng, một lần với mỗi hộp thuốc thử và sau mỗi lần chuẩn. Khoảng cách giữa các lần chạy mẫu chứng và giá trị giới hạn nên tùy thuộc vào yêu cầu riêng của từng phòng thí nghiệm. Kết quả mẫu chứng phải nằm trong thang. Mỗi phòng xét nghiệm nên thiết lập các biện pháp hiệu chỉnh nếu các giá trị mẫu chứng nằm ngoài thang đo.
Nếu cần tiến hành đo lại các mẫu có liên quan
Tuân thủ các quy định chính phủ và hướng dẫn của địa phương về kiểm tra chất lượng.
Lưu ý:
Vì lý do kỹ thuật, phải nhập bằng tay các giá trị đích mới gán cho thuốc thử và mẫu chứng đặc hiệu cho mỗi lô vào tất cả máy phân tích (trừ trường hợp máy cobas e 602). Vì thế luôn xem kỹ tờ giá trị đính kèm trong hộp thuốc thử hay hộp mẫu chứng PreciControl để đảm bảo sử dụng đúng giá trị đích.
Khi sử dụng lô thuốc thử hay lô mẫu chứng mới, máy sẽ sử dụng giá trị gốc được mã hóa trên mã vạch mẫu chứng.
Tính toán
Máy phân tích tự động tính toán ngưỡng phản ứng dựa trên kết quả đo Cal1 và Cal2.
Kết quả của một mẫu có thể biểu thị dưới dạng có phản ứng hoặc không có phản ứng cũng như dưới dạng chỉ số ngưỡng (tín hiệu mẫu/ngưỡng phản ứng).
Yếu tố hạn chế - ảnh hưởng
Xét nghiệm không bị ảnh hưởng bởi bệnh vàng da (bilirubin < 428 µmol/L hoặc < 25 mg/dL), tán huyết (Hb < 1.0 mmol/L hoặc < 1.6 g/dL), lipid huyết (Intralipid < 1000 mg/dL), và biotin < 123 nmol/L hoặc < 30 ng/mL.
Tiêu chuẩn: Chỉ định đúng mẫu âm tính và dương tính.
Ở bệnh nhân dùng liều cao biotin (nghĩa là > 5 mg/ngày), không nên lấy mẫu cho đến ít nhất 8 giờ sau khi dùng liều biotin cuối.
Kết quả xét nghiệm không bị nhiễu bởi các yếu tố thấp khớp với nồng độ lên đến 676 IU/mL.
Thử nghiệm in vitro được tiến hành trên 19 loại dược phẩm thường sử dụng. Không có hiện tượng nhiễu tới xét nghiệm.
Trong một số hiếm trường hợp, nhiễu có thể xảy ra do nồng độ kháng thể kháng kháng thể đặc hiệu kháng chất phân tích (như HAMA) hay ruthenium quá cao của mẫu phẩm phân tích. Xét nghiệm đã được thiết kế phù hợp để giảm thiểu các hiệu ứng này.
Trong một số trường hợp cá biệt, nồng độ kháng thể kháng streptavidin quá cao và gây nhiễu.
Với mục tiêu chẩn đoán, kết quả xét nghiệm cần được đánh giá kèm theo bệnh sử, thăm khám lâm sàng và các phát hiện khác.
Giới hạn đo và khoảng đo
Giới hạn phát hiện: ≤ 0.8 PEI U/mL
Độ nhạy đã công bố được xác định bằng cách đọc nồng độ kháng thể kháng HBc tương ứng với tín hiệu giá trị ngưỡng từ đường chuẩn thu được bằng cách pha loãng theo trình tự mẫu tham chiếu kháng thể kháng HBc trong huyết thanh người không có vi rút viêm gan B của Viện Paul-Ehrlich.
Pha loãng
Có thể sử dụng Elecsys Diluent Universal hoặc huyết thanh người, huyết tương và huyết thanh bào thai bê để pha loãng mẫu.
http://kimhung.vn/vi/shops/Bang-chi-dau-xuong-Elecsys/Hoa-chat-mien-dich-Roche-1710/
TÀI LIỆU ANTI - HBC


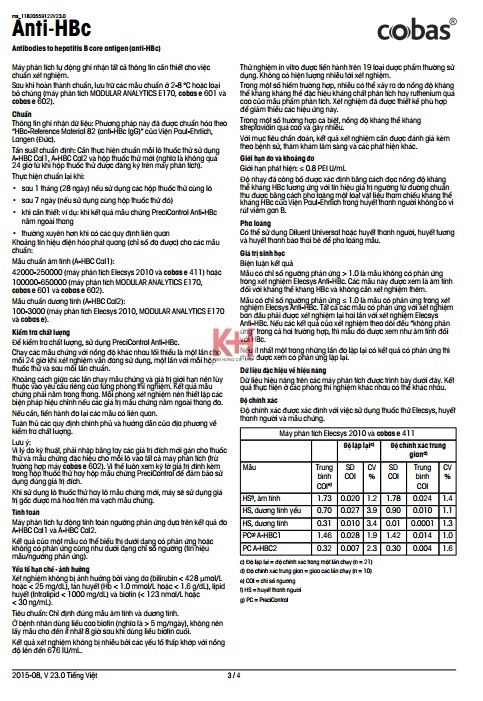
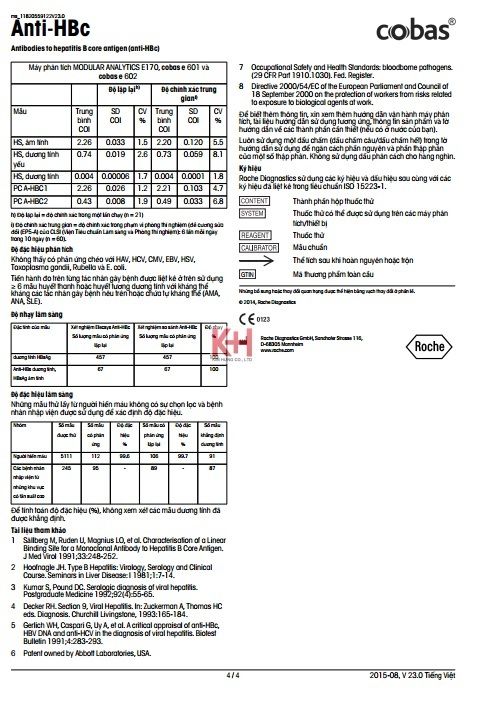
TÀI LIỆU PRECICONTROL - HBC


HẾT HẠN
| Mã số : | 12205794 |
| Địa điểm : | Hà Nội |
| Hình thức : | Cần bán |
| Tình trạng : | Hàng mới |
| Hết hạn : | 16/03/2017 |
| Loại tin : | Thường |








Bình luận